Was bedeutet regulatorische Sicherheit bei sfm medical devices und warum ist sie wichtig?
Bei sfm medical devices geht regulatorische Sicherheit über das formale Pflichtprogramm der Regularien hinaus. Sie ist die Grundlage für Vertrauen, Verlässlichkeit und nachhaltige Innovationsfähigkeit und resultiert aus einem über Jahrzehnte gewachsenen Qualitäts- und Verantwortungsverständnis. Dies ist gerade in der Medizintechnik essenziell.
Regulatorische Sicherheit ist unsere Antwort auf die stetig steigenden regulatorischen Anforderungen
Die vergangenen Jahre haben gezeigt: Die regulatorischen Anforderungen entwickeln sich schneller und komplexer als je zuvor. EU MDR, internationale Zulassungen, steigende Erwartungen an Post-Market-Surveillance, Cyber- und Produktsicherheit sowie immer höhere Dokumentationsanforderungen prägen den Alltag. Unsere Antwort darauf ist kein Aktionismus, sondern Systematik und Verantwortung, welche unsere Prozesse, Strukturen und Entscheidungen prägt.
Regulatorische Sicherheit ist bei sfm Teil des Systems
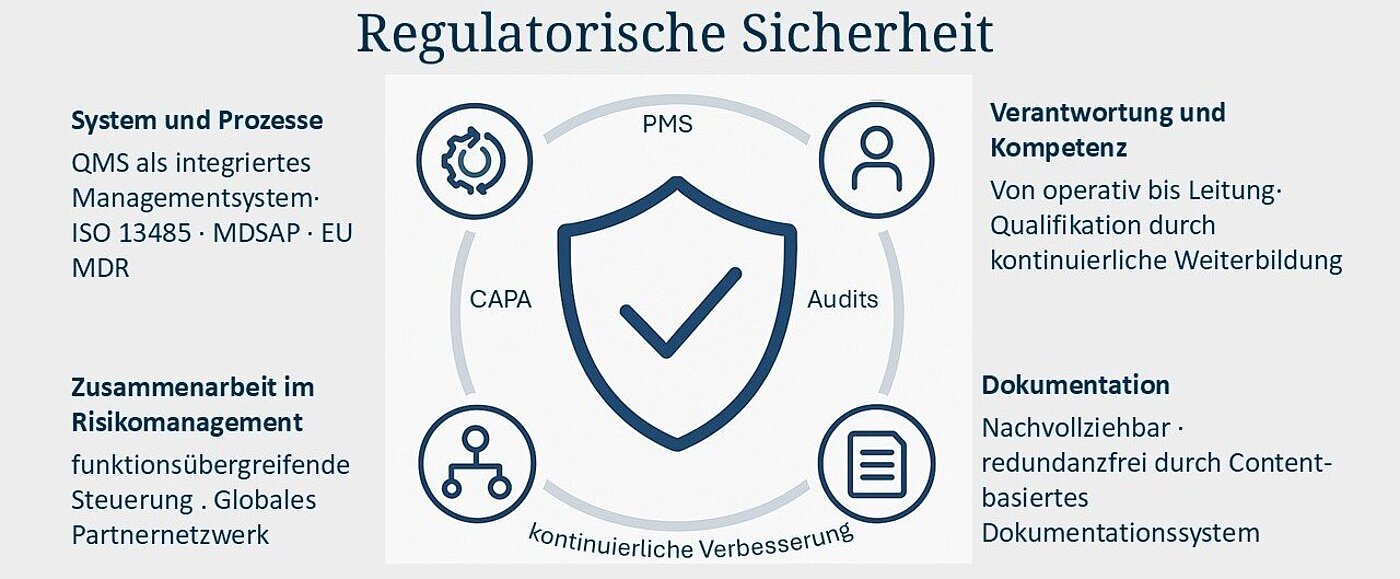
Regulatorische Sicherheit entsteht nicht durch Einzelmaßnahmen, sondern durch ein gelebtes Gesamtsystem. Das Qualitätsmanagementsystem von sfm ist gezielt auf die ISO 13485 und auf MDSAP (Medical Device Single Audit Program) ausgerichtet und seit Jahren auf internationale regulatorische Anforderungen ausgelegt – von Europa über Nordamerika bis in asiatische und weitere globale Märkte.
Entscheidend ist dabei nicht die bloße Erfüllung von regulatorischen Anforderungen, sondern deren stringente Integration in alle Prozesse über den gesamten Lebenszyklus des Medizinprodukts – von der Entwicklung bis zur Überwachung nach dem Inverkehrbringen (Post-Market-Surveillance).
Regulatorische Sicherheit bedeutet für uns:
klar definierte Verantwortlichkeiten (u. a. PRRC / VPR),
ein strukturiertes, risikobasiertes Qualitätsmanagementsystem und
eine belastbare technische Dokumentation über den gesamten Produktlebenszyklus hinweg.


Wie wird die regulatorische Sicherheit bei sfm überprüft und weiterentwickelt?
Regulatorische Sicherheit ist bei sfm “Chefsache“: Sie wird regelmäßig bewertet, kritisch hinterfragt und gezielt weiterentwickelt. Wir betrachten Auditergebnisse, Reklamationen, CAPAs, neue regulatorische Anforderungen und Ressourcenbedarfe nicht isoliert, sondern systematisch verknüpft. Gerade in einem Umfeld wachsender internationaler Zulassungen ist diese Gesamtsicht entscheidend. Sie ermöglicht uns die richtige Priorisierung, schafft Transparenz und stellt sicher, dass regulatorische Entscheidungen risikobasiert, faktenorientiert und nachhaltig getroffen werden.
Regulatorische Sicherheit - eine gemeinsame Verantwortung bei sfm
Kompetenz entsteht durch Wissen. Deswegen liegt bei uns ein Fokus auf regelmäßigen Schulungen, strukturiertem Wissenstransfer, Aufgabenteilung und Einbindung neuer Kolleg:innen mit Wirksamkeitsprüfungen durch die erfahrenen „alten Hasen“. So stellen wir kontinuierlich sicher, dass regulatorische Anforderungen nicht nur bekannt sind, sondern verstanden und angewendet werden – über Bereichsgrenzen hinweg.
Welche Bedeutung hat „Made in Germany” für die regulatorische Sicherheit von sfm?
„Made in Germany“ steht bei uns nicht nur für Präzision und Ingenieurskunst in Bezug auf unsere Medizinprodukte, sondern auch für robuste regulatorische Exzellenz in einem hochdynamischen globalen Umfeld. Um nicht im Anforderungsdschungel unterzugehen, konzentrieren wir uns auf unser bewährtes Produktportfolio - sterile Einmalkanülen und Transfersysteme. Unser Fokus liegt darauf, alle regulatorischen Anforderungen bereits in der Entwicklung zu identifizieren und zu berücksichtigen - nicht am Ende; nicht „irgendwann später“; sondern von Anfang an. Das ist effektiv, schafft Effizienz, vermeidet Fehler und sorgt dafür, dass unsere Medizinprodukte sicher, marktfähig und langfristig für uns und unsere Kunden erfolgreich sind.
Wir schaffen regulatorische Klarheit, reduzieren Risiken und geben Ihnen die Sicherheit, sich auf Ihr Kerngeschäft zu konzentrieren.
Sie suchen einen regulatorisch sicheren Partner für sterile Einmalprodukte, der EU MDR und globale Zulassungen nicht als „Pflichtprogramm“, sondern als System lebt?
Dann schreiben Sie uns- wir sichern Ihre Produkte von Anfang an ab.